Los investigadores han logrado por primera vez mejorar la función del corazón en la insuficiencia cardiaca con la ayuda de un ácido nucleico sintético, según informan en la revista ‘Science Translational Medicine‘.
Los pacientes con insuficiencia cardíaca suelen tener dificultad para respirar y se fatigan rápidamente. A menudo sufren retención de líquidos, palpitaciones y mareos. La enfermedad puede desencadenarse por una combinación de presión arterial elevada, diabetes y enfermedad renal, o por acontecimientos agudos como infartos o infecciones. A medida que las personas envejecen aumenta el número de factores adversos, por lo que la insuficiencia cardíaca afecta principalmente a las personas mayores, especialmente a las mujeres.
Aunque los síntomas son similares, hay varias causas. En una de las formas de la enfermedad, la función de bombeo del corazón se ve afectada. Sin embargo, esto puede mejorarse con una medicación ampliamente disponible. En la otra forma, el corazón bombea con la fuerza adecuada, pero las cámaras del corazón -los ventrículos- no se llenan correctamente porque las paredes ventriculares se engrosan o se vuelven rígidas.
Actualmente no existe ningún tratamiento eficaz para esta forma de insuficiencia cardíaca. Junto con colegas de la Universidad de Heidelberg y la empresa californiana Ionis Pharmaceuticals, un equipo dirigido por el profesor Michael Gotthardt, del Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC), en Alemania, ha desarrollado ahora un agente terapéutico para mejorar el tratamiento de la insuficiencia cardíaca con fracción de eyección preservada.
La mecánica del corazón depende de una proteína gigante elástica llamada titina. Las células del músculo cardíaco la producen en distintas variantes o isoformas que difieren en su flexibilidad.
Mientras que en los bebés predominan las proteínas de titina muy elásticas, más adelante, cuando se completa el crecimiento y la remodelación, se producen isoformas de titina más rígidas para aumentar la eficacia del bombeo.
En la insuficiencia cardíaca con fracción de eyección preservada, el engrosamiento de las paredes cardíacas, el tejido conectivo intercalado y los filamentos de titina más rígidos pueden conducir a una alteración del llenado de los ventrículos.
Las células del músculo cardíaco son prácticamente incapaces de renovarse en los adultos. Sin embargo, la constante actividad de bombeo del músculo cardíaco somete a la titina a una tensión tan severa que las proteínas desgastadas deben romperse y sustituirse cada tres o cuatro días.
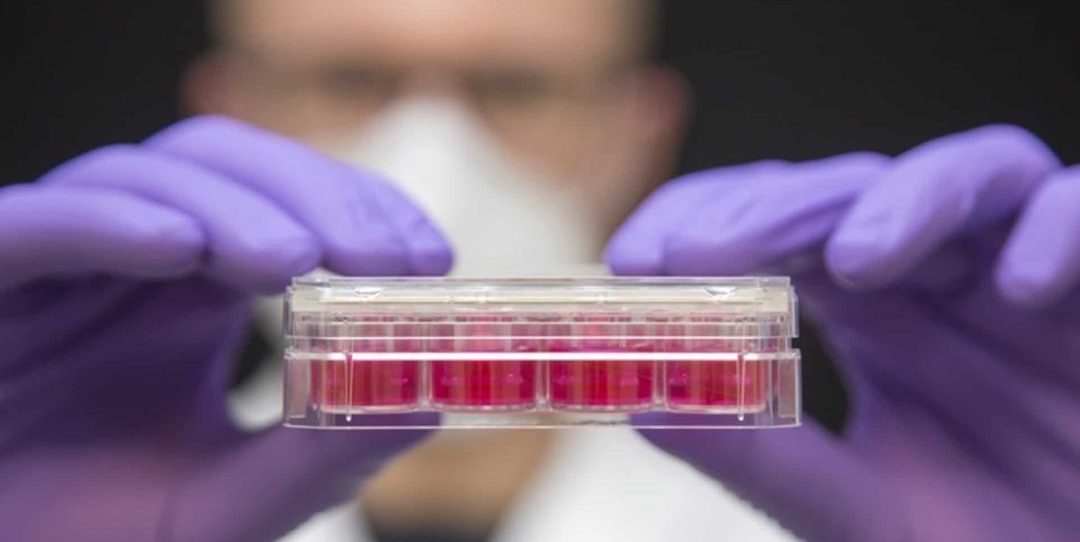
Víctor Badillo Lisakowski cultivó células de músculo cardíaco derivadas de células madre humanas para convertirlas en tejido cardíaco artificial.
«Las propiedades mecánicas de las proteínas de titina son difíciles de ajustar –explica Gotthardt–. Pero ahora podemos intervenir en el proceso que precede a la síntesis de la proteína: es el empalme alternativo».
El empalme alternativo es un truco que la naturaleza ha ideado para crear una variedad de proteínas similares a partir de un único gen, incluidas las diferentes formas de titina. Este proceso está controlado por factores de empalme. «Uno de ellos, el regulador maestro RBM20, es una diana adecuada a la que podemos dirigirnos terapéuticamente», explica Gotthardt.
El RBM20 determina las propiedades elásticas, contráctiles y eléctricas de las cámaras del corazón. Que es efectivamente el factor decisivo se demostró en experimentos preliminares con ratones que, debido a una deleción, pueden producir sólo la mitad de RBM20 que los ratones normales: En los ratones deficientes, se produjo un cambio hacia isoformas de titina más elásticas. Junto con los investigadores de Ionis, los científicos empezaron a buscar una forma de influir en la RBM20.
«Nos sorprendió lo fácil que era hacerlo», recuerda Gotthardt, concretamente con oligonucleótidos en antisentido (OAS). Se trata de cadenas cortas de ácidos nucleicos monocatenarios que se producen sintéticamente. Se unen específicamente a la secuencia complementaria de ARN, el plano de la proteína objetivo, bloqueando así su síntesis.
El doctor Michael Radke, autor principal del estudio, probó primero con éxito los OAS en ratones con paredes cardíacas más rígidas. A continuación, su colega Víctor Badillo Lisakowski cultivó células de músculo cardíaco derivadas de células madre humanas para convertirlas en tejido cardíaco artificial.
Las diminutas estructuras en 3D pueden ser estimuladas para contraerse y relajarse cuando encuentran resistencia, lo que les permite imitar la acción de bombeo del corazón. Este tejido cardíaco artificial también demostró el efecto del tratamiento: Los investigadores pudieron demostrar que las moléculas de OAS penetran realmente en las células y desencadenan la respuesta deseada.
«Estas pruebas en tejido cardíaco artificial fueron un paso importante, porque las secuencias primarias de la titina no son idénticas en los ratones y en los humanos», dice Radke.
Por primera vez se han utilizado con éxito oligonucleótidos antisentido para influir terapéuticamente en el empalme alternativo de las enfermedades cardíacas. Los investigadores de Ionis lograron estabilizar la molécula sensible de forma que llegara a los músculos estriados del modelo de ratón y no se degradara en la sangre, el hígado o fuera eliminada por los riñones.
La mayor parte termina en el corazón, y una parte entra en el músculo esquelético. «En el modelo de ratón, sin embargo, observamos que no tiene ningún efecto perturbador el aumento de las cantidades de titina elástica en el músculo esquelético», subraya Radke.
La insuficiencia cardíaca es una enfermedad crónica que requiere un tratamiento a largo plazo. «Así que tratamos a nuestros ratones durante un periodo de tiempo más largo y pudimos ver efectos duraderos del tratamiento», dice Gotthardt. Señala que el enfoque terapéutico aún necesita algo de trabajo, y añade que «una mejora respecto a una inyección semanal, con la que muchos pacientes ya están familiarizados por la insulina o la heparina, sería la administración oral».